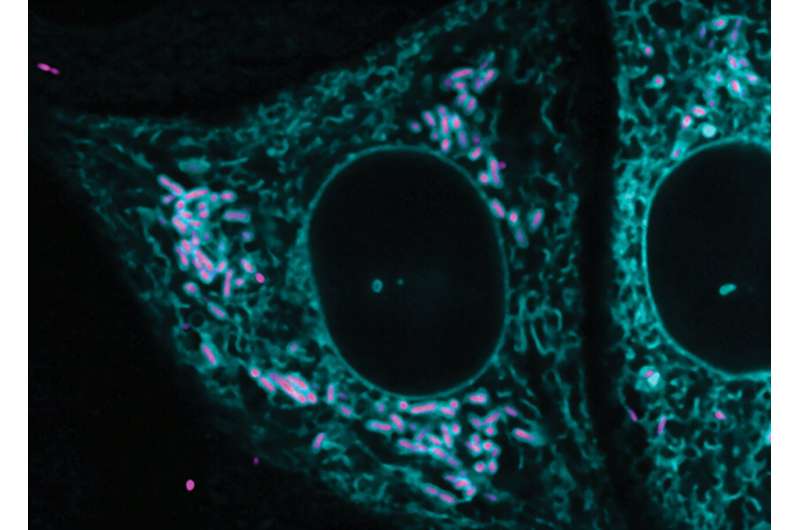
Bakteri R. parkeri (magenta) mund të shihet këtu duke formuar kontakte të drejtpërdrejta ndërmjet mbretërive me retikulumin endoplazmatik të ashpër (cian), shembulli i parë i njohur i një patogjeni brendashqisor që ndërvepron me një membranë eukariote në këtë mënyrë. Kredite: Lamason Lab.
Në tekstet shkollore të biologjisë, retikulumi endoplazmatik shpesh paraqitet si një organelë e veçantë dhe kompakte pranë bërthamës dhe zakonisht njihet për rolin e tij në trafikimin dhe sekretimin e proteinave. Në realitet, retikulumi endoplazmatik është i gjerë dhe dinamik, i shpërndarë nëpër qelizë dhe i aftë të krijojë kontakte dhe komunikim me dhe ndërmjet organelave të tjera. Këto kontakte membranore rregullojnë procese aq të ndryshme sa metabolizmi i yndyrave, metabolizmi i sheqerit dhe përgjigjet imunitare.
Studimi se si patogjenët manipulojnë dhe uzurpojnë proceset jetike për të promovuar ciklet e tyre të jetës mund të zbulojë shumë për funksionet themelore qelizore dhe të ofrojë njohuri për opsione të mundshme trajtimi për patogjenët ende të pastudiuar.
Hulumtime të reja nga Lamason Lab në Departamentin e Biologjisë në MIT, të publikuara së fundmi në Journal of Cell Biology, kanë treguar se patogjeni bakterial Rickettsia parkeri, i cili jeton lirshëm në citosol, mund të ndërveprojë në mënyrë të gjerë dhe të qëndrueshme me retikulumin endoplazmatik të ashpër, duke formuar kontakte të papara më parë me këtë organelë.
Është shembulli i parë i njohur i një vendi kontakti të drejtpërdrejtë ndërmjet mbretërive ndërmjet një patogjeni bakterial brendashqisor dhe një membrane eukariote.
Laboratori Lamason studion R. parkeri si një model për infeksionin nga Rickettsia rickettsii, një bakter më virulent. R. rickettsii, i bartur dhe transmetuar nga rriqrat, shkakton ethet e njollosura të Maleve Shkëmbore (Rocky Mountain Spotted Fever). Nëse nuk trajtohet, infeksioni mund të shkaktojë simptoma aq të rënda sa dështimi i organeve dhe vdekja.
Rickettsia është e vështirë për t’u studiuar sepse është një patogjen obligativ, që do të thotë se mund të jetojë dhe të riprodhohet vetëm brenda qelizave të gjalla, ashtu si një virus. Studiuesit duhet të jenë kreativë për të analizuar pyetjet themelore dhe lojtarët molekularë në ciklin jetësor të R. parkeri, dhe shumë gjëra mbeten të paqarta rreth mënyrës se si përhapet R. parkeri.
Devijimi drejt lidhjeve
Autorja e parë, Yamilex Acevedo-Sánchez, një ish-studente e programit BSG-MSRP-Bio dhe një studente e diplomuar në atë kohë, hasi në ndërveprimet mes retikulumit endoplazmatik dhe R. parkeri ndërsa përpiqej të vëzhgonte Rickettsia që arrinte në një lidhje qelizore.
Modeli aktual për infeksionin nga Rickettsia përfshin R. parkeri që përhapet qelizë më qelizë duke udhëtuar në vendet e specializuara të kontaktit midis qelizave dhe duke u kapur nga qeliza fqinje për t’u përhapur. Listeria monocytogenes, të cilën gjithashtu e studion Lamason Lab, përdor bishtet e aktinës për të lëvizur me forcë në një qelizë fqinje. Në kontrast, R. parkeri mund të formojë një bisht aktine, por e humbet atë para se të arrijë lidhjen qelizore. Megjithatë, R. parkeri ende është në gjendje të përhapet në qelizat fqinje.
Pas një seminari në MIT mbi funksionet më pak të njohura të retikulumit endoplazmatik, Acevedo-Sánchez zhvilloi një linjë qelizore për të vëzhguar nëse Rickettsia mund të përhapej në qelizat fqinje duke u “shfrytëzuar” nga retikulumi endoplazmatik për të arritur në lidhjen qelizore.
Në vend të kësaj, ajo pa një përqindje të papritur të lartë të R. parkeri të rrethuar dhe të mbështjellë nga retikulumi endoplazmatik, në një distancë prej rreth 55 nanometrash. Kjo distancë është e rëndësishme sepse kontaktet e membranës për komunikimin ndërmjet organelave në qelizat eukariote formojnë lidhje që janë nga 10 deri në 80 nanometra të gjera. Studiuesit përjashtuan që ajo që panë nuk ishte një përgjigje imune dhe seksionet e retikulumit endoplazmatik që ndërvepronin me R. parkeri ishin ende të lidhura me rrjetin më të gjerë të retikulumit.
“Jam e mendimit se, nëse dëshiron të mësosh biologji të re, thjesht shiko qelizat,” thotë Acevedo-Sánchez. “Manipulimi i organelës që krijon kontakte me organela të tjera mund të jetë një mënyrë e shkëlqyer për një patogjen që të marrë kontroll gjatë infeksionit.”
Lidhje të qëndrueshme
Lidhjet e qëndrueshme ishin të papritura sepse retikulumi endoplazmatik është vazhdimisht duke prishur dhe duke rikrijuar lidhje, të cilat zgjasin sekonda ose minuta. Ishte surprizë të shihje retikulumin endoplazmatik të lidhej në mënyrë të qëndrueshme përreth bakterit. Si një patogjen citosolik që ekziston lirshëm në citosolin e qelizave që infekton, ishte gjithashtu e papritur të shihej R. parkeri i rrethuar nga një membranë.
Përkufizime të qarta
Acevedo-Sánchez bashkëpunoi me Qendrën për Sistemet Nanoskopike në Universitetin e Harvardit për të parë vëzhgimet e saj fillestare me rezolucion më të lartë duke përdorur mikroskopinë elektronike me rreze të përqendruar jonike (FIB-SEM). Ky proces përfshin marrjen e një kampioni qelizash dhe shpërthimin e tyre me një rreze të përqendruar jonesh për të hequr një pjesë të bllokut të qelizave. Me çdo shtresë, merret një imazh me rezolucion të lartë.
Nga aty, Acevedo-Sánchez identifikoi zonat e ndryshme të imazheve—si mitokondritë, Rickettsia ose retikulumi endoplazmatik—dhe një program quajtur ORS Dragonfly, një program i mësimit makinerik, analizoi mijëra imazhe për të identifikuar këto kategori. Kjo informacion më pas u përdor për të krijuar modele 3D të mostrave.
Përfundim
Lidhjet e identifikuara midis R. parkeri dhe retikulumit endoplazmatik hapin një dritare të re në mënyrën se si patogjenët mund të manipulojnë qelizat gjatë infeksionit. Ndërveprime të tilla mund të zbulojnë mënyra të reja për trajtimin e infeksioneve dhe për të kuptuar më mirë biologjinë qelizore.